Муковисцидоз — это тяжелое наследственное хроническое заболевание, возникающее вследствие мутации белка, принимающего участие в перемещении хлорид-ионов через клеточную мембрану, в результате чего поражаются железы внешней секреции, продуцирующие пот и слизь. Нельзя преуменьшать роль слизи в организме человека: она увлажняет и защищает органы от высыхания и инфицирования патогенными бактериями. Таким образом, нарушения выработки слизи лишают человека одного из важнейших механических барьеров. Муковисцидоз неизлечим и неминуемо приводит к серьезнейшим нарушением деятельности внутренних органов.
Что же означает сам термин «муковисцидоз», если его препарировать на составные части? «Мукус» — это слизь, «висцидус» — вязкая, что на сто процентов соответствует сущности болезни. Тягучая, липкая слизь собирается в поджелудочной железе и бронхах, буквально «забивает», закупоривает их. Застойная слизь — благоприятная среда для размножения патогенных бактерий. Поражаются также желудочно-кишечный тракт, придаточные пазухи носа, почки и весь мочеполовой тракт.
Что такое муковисцидоз
Муковисцидоз – это хроническое генетическое заболевание. По-другому патологию называют «кистозный фиброз».
Болезнь не возникает внезапно у мужчин или у женщин во взрослом возрасте. Диагноз ставят вскоре после рождения. Так как с болезнью уже рождаются, она не может передаться окружающим людям.
Важно! Примерно у 4% всех пациентов с муковисцидозом болезнь удается диагностировать у взрослых людей, а весь период до этого патология носит бессимптомный характер.
Обычно патологию выявляют еще у грудничка. Когда болезнь удалось определить у детей до года, возрастают шансы сохранить и продлить жизнь ребенку. Раньше при данном заболевании пациенты вскоре погибали. Однако сейчас, хотя вылечить заболевание по-прежнему невозможно, при правильной терапии продолжительность жизни людей с таким диагнозом составляет до 35-45 лет.
Муковисцидоз у новорожденных налагает отпечаток на всю жизнь человека. Симптоматика затрагивает разные сферы здоровья. Это связано с тем, что патология поражает не одну систему организма. В патологический процесс постепенно вовлекается пищеварительная, дыхательная, половая, кишечная и другие системы.
Сам термин «муковисцидоз» происходит от двух латинских слов, означающих «слизь» и «липкий». Именно это и происходит со всеми жидкостями наружной секреции: они густеют, застаиваются и приводят к нарушениям в органах.
Причины муковисцидоза
Основная причина муковисцидоза — это наследственная патология, которая возникает в результате мутации гена — трансмембранного регулятора муковисцидоза. Этот ген участвует в обмене эпителиальных тканей, выстилающих пищеварительный тракт, печень, поджелудочную железу, репродуктивные и бронхолегочные органы. Мутация гена приводит к нарушению структуры синтезируемого белка, он становится вязким и густым. Из-за застоя слизи и повышения в ней уровня хлора и натрия, эпителий желез начинает уменьшаться в размере, замещаться соединительной тканью.
Скопление слизи создает благоприятные условия для размножения условно-патогенной флоры, поэтому резко возрастает риск возникновения гнойных осложнений и сопутствующих заболеваний. При муковисцидозе у взрослых значительно страдает репродуктивная функция.
Механизм развития болезни
Первые признаки муковисцидоза могут появиться у ребенка только в полугодовалом возрасте. Однако возникновение болезни происходит из-за того, что оба родителя передают ген, подвергшийся мутации, который отвечает за нормальную выработку жидкостей, продуцируемых разными железами организма.
Тип наследования муковисцидоза – аутосомно-рецессивный. Чтобы ребенок заболел, нарушенный ген должны передать и отец, и мать. При передаче гена только лишь одного из родителей, наступает носительство, однако заболевание не начинается.
Формы муковисцидоза
Рассматриваемое нами заболевание характеризуется множеством различных проявлений, для него актуальных, при этом все они определяются степенью выраженности патологических изменений, актуальностью осложнений, а также возрастом больного. Формы муковисцидоза могут быть следующие:
- преимущественным образом легочная (бронхолегочная или респираторная);
- преимущественным образом кишечная;
- смешанная (в данном случае поражению подлежит одновременно и органы дыхания, и ЖКТ);
- мекониевая непроходимость кишечника;
- стертые и атипичные варианты форм проявления заболевания.
Указанное деление муковисцидоза на формы является условным, потому как указание преимущественно легочного поражения сопоставляется с актуальными нарушениями органов пищеварения, в то время как кишечное поражение сопровождается развитием соответствующих изменений в бронхолегочной системе. Важно отметить и то, что для заболевания характерно разнообразие его клинических проявлений в каждом отдельном случае его возникновения. Поражению подвергаются многие органы, но в наибольшей степени страдают именно легкие, кишечник, поджелудочная железа и печень. Между тем, одной из наиболее важных особенностей муковисцидоза является и то, что умственные способности больных ни в коей мере не затрагиваются.
Стертые и атипичные формы заболевания могут быть выявлены в результате обследования на предмет актуальности хронического синусита у ребенка. В более старшем возрасте муковисцидоз может быть выявлен при актуальном для мужчин бесплодии. Бесплодие у мужчин вне зависимости от формы заболевания является его сопутствующей патологией. Оно провоцирует азооспермию (отсутствие сперматозоидов в семенной жидкости), азооспермия, в свою очередь, развивается из-за атрофии семенного канатика (т.е. из-за уменьшения его в размерах или из-за поражения его тканей, за счет чего нарушаются/прекращаются свойственные ему функции), из-за его врожденного отсутствия или в результате обструкции (т.е. нарушения проходимости). Указанные нарушения могут также встречаться у тех пациентов, которые являются лишь носителями гена муковисцидоза.
Муковисцидоз у женщин проявляется в снижении фертильности (способности к воспроизводству потомства), обуславливается это повышенной степенью вязкости, актуальной для отделяемого маточным цервикальным каналом, за счет чего усложняется возможность миграции сперматозоидов.
Причины болезни
Основной причиной развития данного заболевания – генная мутация. Именно из-за этого болезнь считается неизлечимой.
Причины, из-за которых пациенты ощущают широкий спектр симптомов, сводятся к следующим:
- нарушение секреции нормальной мокроты;
- избыток кальция и хлорида натрия в выделяемых жидкостях;
- скопление мукополисахаридов.
Под воздействием этой группы факторов развиваются осложнения, связанные с мутацией генов.
МУКОВИСЦИДОЗ: СОВРЕМЕННЫЙ ПОДХОД К ДИАГНОСТИКЕ И ЛЕЧЕНИЮ
В последнее время достигнут определенный прогресс в научном подходе к муковисцидозу в результате достижений в области клеточной патологии, генетики и молекулярной биологии. Эта статья представляет собой обзор текущего состояния проблемы муковисцидоза и затрагивает основные причины, тип наследования, современную терапию и новые достижения в изучении этой патологии.
Cystic fibrosis (CF) is one of the most common autosomal recessive inherited disorders in the European population and represents an important cause of morbidity and mortality among children and young adults. In the past decades the number of the CF patients has increased considerably due to improved diagnosis and a more comprehensive approach to therapy. Recently, the scientific knowledge about CF has been improved as the result of advances in cell pathology, genetics and molecular biology. This article reiews the current status of our understanding of CF: and covers the main causes, mode of inheritance, current therapy and new approaches to the pulmonary disease.
Е. Л. Амелина, А. Г. Чучалин НИИ пульмонологии Минздрава РФ, Москва
Ye. L. Amelina, A. G. Chuchalin Pulmonology, Ministry of Health of the Russian Federation, Moscow
М
уковисцидоз (МВ) — наследственное заболевание, обусловленное системной дисфункцией экзокринных желез. Болезнь впервые была описана сравнительно недавно, в 1938 г. Патологоанатом Дороти Андерсен описала кистозную дегенерацию поджелудочной железы в сочетании с легочной патологией у маленьких детей [1]. Тогда возникло английское название болезни — Cystic fibrosis (кистозный фиброз). В 1946 г. Farber предложил термин «муковисцидоз» (от лат. mucus — слизь, viscus — вязкий), указывая на роль повышения вязкости экскрета, выделяемого экзокринными железами. Однако еще раньше, в старинных немецких сказаниях, указывалось, что если при поцелуе ребенка ощущается соленый привкус — ребенок обречен [2].
Н-нормальный ген М-ген муковисцидоза
Рис. 1. Аутосомно-рецессивный тип наследования при МВ.
За последние годы стремительно развивалось научное знание о МВ, механизме его развития на клеточном и молекулярном уровне. В настоящее время известно, что МВ является самым частым моногенным заболеванием среди европейцев. Каждый 25-й представитель европейской расы является носителем гена МВ. Распространенность МВ наиболее высока в Центральной Европе — 1 больной ребенок на 2000 родов [3]. Эпидемиологические исследования по частоте случаев МВ в России установили противоречивые данные — от 1 : 3860 новорожденных [4] до 1:12 300 [5].
Рис. 2. Механизм транспорта ионов через апикальную мембрану эпителиальной клетки при МВ.
Прогресс в диагностике и лечении МВ привел к значительным изменениям продолжительности жизни при этом заболевании. В 1938 г. 70% заболевших погибали в течение первого года жизни. В 1996 г. средняя продолжительность жизни больных МВ в США и странах Западной Европы достигла 29 лет. Аналогичный показатель по России составляет лишь 16 лет [6]. В центре МВ взрослых на базе Brompton Hospital наблюдали пациента, достигшего возраста 72 лет. Такое отставание связано с недостаточным развитием общенациональной сети специализированных центров МВ, отсутствием самостоятельной клиники МВ взрослых.
Этиология и патогенез
МВ развивается в результате мутации гена, расположенного на длинном плече седьмой хромосомы. Тип наследования — аутосомно-рецессивный (рис. 1). В настоящее время известно более 400 мутаций, из которых в Европе и России наиболее часто встречается мутации F 508 (потеря аминокислоты финилаланина в позиции 508). Подобное изменение структуры ДНК приводит к нарушению функции трансмембранного регулятора МВ (МВТР) — белка, обеспечивающего транспорт иона хлора через апикальную часть мембраны эпителиальной клетки (рис. 2). Вследствие этого дефекта анионы хлора задерживаются в клетке, усиливают абсорбцию катионов натрия и воды, «высушивая» слизь, продуцируемую экзокринными железами. Увеличение вязкости экскрета приводит к закупориванию протоков экзокринных желез, накоплению экскрета и образованию кист. Развивается картина системной дисфункции экзокринных желез. Поражаются те органы, в эпителиальных клетках которых нарушена функция хлоридных каналов. Это — верхние и нижние дыхательные пути, потовыводящие протоки, выводные протоки слюнных желез, поджелудочной железы, желчевыводящие пути, кишечник, семявыносящие протоки. Из-за блокады хлоридных каналов не происходит реабсорбция ионов хлора и натрия в потовыводящих протоках, что приводит к значительному повышению концентрации этих ионов в 1 мл пота. Этот феномен используется при диагностике МВ. Следует также помнить, что в жаркое время года у таких больных при физической нагрузке происходит значительная потеря электролитов, что может привести к коллапсу. Поражение поджелудочной железы, вызванное закупориванием ее протоков густым, вязким секретом, приводит к образованию кист и в дальнейшем к кистозно-фиброзному перерождению паренхимы поджелудочной железы. В результате развивается внешнесекреторная недостаточность поджелудочной железы с явлениями стеатореи, мальабсорбции с сопутствующей недостаточностью жирорастворимых витаминов А, D, E, К , отставанием в физическом развитии. В более старшем возрасте из-за фиброзного перерождения стромы поджелудочной железы и при поражении островков Лангерганса развивается эндокринная недостаточность поджелудочной железы, приводящая к формированию сахарного диабета .
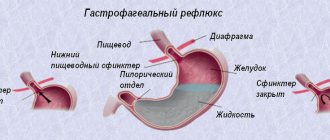
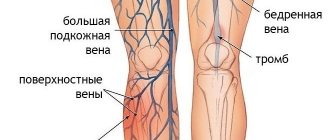
Поражение желчевыводящих протоков приводит к развитию билиарного цирроза с портальной гипертензией, выражающейся в варикозном расширении вен пищевода (возможно с кровотечением из них), асцитом, спленомегалией и гиперспленизмом. У всех больных МВ при ультразвуковом исследовании можно выявить картину холестаза, у 15% на этом фоне формируются камни желчного пузыря [7].
Рис.3. Обзорная рентгенограмма больного В., 15 лет, во время обострения хронического гнойно-воспалительного процесса в легких (а) и после курса в/в антибактериальной терапии (б). Уменьшилась очаговая и перибронхиальная инфильтрация, однако сохраняются грубое усиление и деформация легочного рисунка, расширение корней легких, гипервоздушность.
Основной механизм поражения кишечника заключается в том, что из-за нарушенного транспорта ионов натрия и хлора содержание электролитов и жидкости в просвете кишечника резко снижено, что может привести к мекониальной кишечной непроходимости в младенчестве, выпадению прямой кишки в детстве, развитию кишечной непроходимости на уровне илеоцекального угла в более старшем возрасте. Двусторонняя атрезия семявыносящих протоков приводит к азооспермии и мужскому бесплодию у 97% больных мужчин [8]. Почти все больные МВ страдают синуситами, у 30% больных выявляется полипоз носа [9]. Патология легких занимает особое место в клинической картине МВ. Именно поражение легких с последующими осложнениями приводит к 70% смертей при МВ [7]. Патологический процесс в легких начинается после рождения ребенка, когда в просвете бронхов формируется густой и вязкий секрет, приводящий к нарушению мукоцилиарного клиренса. Возникающий мукостаз является благоприятной основой для развития инфекционно-воспалительных процессов. Хронический гнойный бронхит,частые бронхопневмонии приводят к формированию ателектазов, бронхиоло-бронхоэктазов, в более позднем возрасте возникают осложнения в виде пневмоторакса, легочного кровотечения. По мере прогрессирования патологических изменений в бронхолегочной системе нарастает вентиляционно-перфузионный дисбаланс, возникает гипоксия, легочная гипертензия и формируется хроническое легочное сердце. Все это ведет к нарастанию дыхательной и сердечно-сосудистой недостаточности, являющейся непосредственной причиной смерти больного.
Клинические проявления
Большое число мутаций, в различной степени воздействующих на количество и качество белка МВТР в эпителиальных клетках, определяет разнообразие клинических проявлений МВ. Клинические проявления МВ могут возникнуть как в раннем младенческом возрасте, так и в более поздний период жизни больного. При относительно благополучном течении болезни МВ может длительно протекать бессимптомно, в некоторых случаях диагноз ставится при обследовании по поводу хронического синусита или мужского бесплодия. В неонатальном периоде обращают на себя внимание незначительное прибавление массы тела, признаки мальабсорбции. В 10% наблюдений МВ начинается с мекониального илеуса в раннем младенчестве [10]. В постнатальном периоде ведущим проявлением МВ становятся повторные бронхолегочные инфекции. Диагноз МВ ставится на основе характерной клинической картины в сочетании с положительным потовым тестом. Классическую диагностическую триаду при МВ составляют:
- положительный потовый тест (хлориды пота более 60 мэкв/л);
- легочная патология инфекционно-воспалительного характера;
- кишечный синдром.
Диагноз подтверждается:
- отягощенным семейным анамнезом;
- положительным результатом генетического анализа;
- повышенным содержанием иммунореактивного трипсина в крови (исследование имеет диагностическое значение при неонатальном скрининге, так как от рождения до 8 нед жизни эти показатели повышены);
- азооспермией, вызванной обструкцией семявыносящих протоков.
При постановке диагноза МВ взрослым следует обратить внимание на характерный вид больного. Это, как правило, молодые пациенты с признаками пониженного питания, небольшого роста, имеющие длительный анамнез хронического бронхита, бронхоэктазов, хронического гайморита или хронического панкреатита. При активном расспросе можно выявить жалобы на диарею, у девушек возможно нарушение менструального цикла. При физикальном исследовании пациента выявляются астеническое телосложение, бочкообразная форма грудной клетки, деформация дистальных фаланг в виде «барабанных палочек». Могут иметь место одышка, акроцианоз. При аускультации над легкими выслушиваются разнокалиберные хрипы. При пальпации живота можно выявить увеличение размеров печени, селезенки. При рентгенологическом исследовании определяется гипервоздушность легких, видны участки инфильтрации или ателектаза, утолщение стенок бронхов, возможна картина пневмоторакса. При проведении компьютерной томографии обнаруживаются множественные бронхоэктазы. Исследования функции внешнего дыхания выявляют обструктивные нарушения в сочетании с увеличением остаточного объема. Возможны также рестриктивные изменения как результат развившегося пневмосклероза. Диффузионная способность легких снижается на более поздних стадиях заболевания за счет гиповентиляции [11]. На электрокардиограмме видны признаки тахикардии, перегрузки правых отделов сердца. Микробиологический анализ мокроты крайне важен для определения возбудителя инфекционного процесса в бронхолегочной системе, для прогноза течения болезни и прицельного назначения антибактериальной терапии. Антибактериальные препараты, рекомендуемые для лечения больных МВ
| Saphilococcus aureus | Клоксациллин | 25 мг/кг/сут |
| Флуклоксациллин | 70 мг/кг/сут | |
| Фузидиновая кислота | 50 мг/кг/сут | |
| Клиндамицин | 20 — 40 мг/кг/сут | |
| Рифампицин | 15 г/кг/сут | |
| Цефалопориновые антибиотики 1-го и 2-го поколения | 100 мг/кг/сут | |
| Pseudomonas aeruginosa | ||
| Профилактика хронической колонизации | Ципрофлоксацин | 20 — 50 мг/кг/сут внутрь |
| Колистин | 1 — 2 млн ЕД в ингаляциях дважды в сутки | |
| Хроническая колонизация | ||
| Лечение обострений (3 нед) | Азлоциллин | 250 — 500 мг/кг/сут внутривенно |
| или | Пиперациллин | 300 мг/кг/сут внутривенно |
| Амикацин | 15 мг/кг/сут внутривенно | |
| плановые курсы | Гентамцин | 8 — 12 мг/кг/сут внутривенно |
| 2 нед каждые 3 мес | Тобрамицин | 10 — 20 мг/кг/сут внутривенно |
| 2 противосинегнойных | Нетилмицин | 10 — 12 мг/кг/сут внутривенно |
| препарата | Цефсулодин | 100 — 150 мг/кг/сут внутривенно |
| Цефтазидим | 100 — 250 мг/кг/сут внутривенно | |
| Азтреонам | 150 — 250 мг/кг/сут внутривенно | |
| Тиенамицин | 50 — 75 мг/кг/сут внутривенно | |
| Ципрофлоксацин | 15 — 50 мг/кг/сут внутрь, внутривенно | |
| Длительная терапия | ||
| Колистин | 1 — 2 млн ЕД в ингаляциях | |
| Гентамицин | 160 — 240 мг дважды в сутки | |
| Тобрамицин | 100 — 300 мг | |
| Карбенициллин | 1 — 2 г |
Микробный пейзаж при МВ достаточно характерен. В раннем детском возрасте доминирует золотистый стафилококк (Staphilococcus aureus), затем присоединяется гемофильная палочка (Наemofilus influaenzae), в подростковом возрасте появляется синегнойная палочка (Pseudomonas aeruginosa). В последние годы, особенно в странах Западной Европы и Америки, часто высевается Pseudomonas cepacia, или Burgholderia cepacia, резистентная к большинству антибиотиков [12]. Присоединение синегнойной инфекции может иметь различные последствия для больного: от бессимптомного носительства до, чаще, значительного ухудшения течения заболевания с выраженной активизацией воспалительного процесса и ухудшением функциональных показателей.
Лечение
На основании клинических, функциональных и микробиологических данных строится тактика лечения МВ. Основной целью проводимой терапии являются:
- уменьшение бронхиальной обструкции;
- борьба с инфекцией;
- улучшение нутритивного статуса больного.
Следует проводить активное лечение сопутствующих осложнений, компенсировать возникающую дыхательную и сердечную недостаточность, обеспечивать максимальный комфорт для больного в терминальном периоде заболевания. В стадии разработки находятся новые, революционные методы лечения МВ (например, генная терапия). Снижение бронхиальной обструкции
проводится при помощи нескольких групп препаратов. Это — муколитики, бронходилататоры в сочетании с приемами кинезитерапии. Муколитики — препараты, уменьшающие вязкость мокроты (N-ацетилцистеин и его аналоги) — применяются в таблетках, ингаляциях и внутривенно. С 1994 г. используется ДНКаза — препарат, расщепляющий ДНК разрушенных нейтрофилов в просвете бронха. Как показали законченные недавно многоцентровые исследования, ежедневные двухкратные ингаляции 2,5 мг препарата приводит к улучшению самочувствия больного, уменьшению числа обострений, улучшению функциональных показателей и в итоге — качества жизни больного [13]. Бронходилататоры также используются для улучшения бронхиальной прходимости. Это — препараты b-агонистов (сальбутамол, сальметерол ) и М-холинолитиков (ипратропиума бромид). Эффективность их применения определяется показателями обратимости обструкции после ингаляции препарата при исследовании функции внешнего дыхания. Бронходилататоры чаще всего используются в комплексе ежедневных процедур, включающих ингаляции муколитиков и упражнения кинезитерапии. Кинезитерапия — это вид физиотерапии, направленный на мобилизацию и эвакуацию мокроты из бронхиального дерева. Наиболее распространенными формами кинезитерапии являются цикл активного дыхания и хаффинг, аутогенный дренаж, постуральный дренаж в сочетании с перкуссионным массажем. Возможно использование флаттера и PEP -маски (positeve expiratory pressure) для создания положительного давления на выдохе и предотвращения экспираторного коллапса [14].
Борьба с инфекцией.
Введение в арсенал терапевтов антибиотиков в 1940 г. было самым значительным событием, изменившим прогноз больных МВ. Антибиотики и сейчас являются краеугольным камнем в лечении этой патологии. Антибактериальная терапия назначается с учетом результата посева мокроты прерывистыми курсами при обострении или в плановом порядке, а также в составе базисной терапии для продления периода ремиссии между обострениями (см. таблицу). Фармакокинетика антибактериальных препаратв при МВ изменена: из-за ускорения метаболизма лекарственных препаратов в печени и увеличения почечного клиренса максимальная концентрация вводимого антибиотика в сыворотке крови больного МВ меньше предполагаемой. Поэтому при МВ требуются большие дозы препарата с максимальной частотой введения. Антибактериальная терапия при МВ опирается на результаты микробиологического исследования мокроты с определением чувствительности к антибиотикам выделенного возбудителя [15]. При лечении обострения препаратами выбора для стафилококковой инфекции являются пенициллиназаустойчивые пенициллины (флуклоксациллин, диклоксациллин), цефалоспорины 1-го и 2-го поколения (цефалексин, цефаклор), используются также доксициклин, клиндамицин, рифампицин,фузидин. В последние годы из мокроты у больных МВ высевается иногда метициллинрезистентный стафилококк. В таком случае препаратом выбора становится ванкомицин. При колонизации синегнойной палочки терапия, как правило, проводится с применением двух противосинегнойных препаратов, внутривенно, курсом не менее 14 дней. Это препараты из группы цефалоспоринов 3 -го поколения (цефтазидим), аминогликозидов (гентамицин, сизомицин, амикацин), карбапенемов (тиенам, меронем). Препарат из группы дифторированных хинолонов — ципрофлоксацин — единственный противосинегнойный препарат, производимый и в таблетированной форме, что очень важно для амбулаторного ведения больных. Лечение обострений начинают при повышении температуры, усилении кашля, усугублении одышки, увеличении количества мокроты. Объективными показателями обострения служат: десатурация кислорода, снижение объема форсированного выдоха в секунду на 10 % и более, изменения в физикальной и рентгенологической картине. Во многих центрах МВ курс внутривенной терапии при носительстве синегнойной палочки проводят каждые 3 мес в плановом порядке. Внутривенная антибактериальная терапия может проводиться не только в условиях стационара, но и на дому. Вне обострения рекомендуется длительная ингаляция противосинегнойных препаратов (колимицин, карбенициллин, гентамицин) для подавления постоянно текущего инфекционного процесса. Длительные исследования эффективности и безвредности ингаляционной антибактериальной терапии доказали стабилизацию клинических проявлений и улучшение функциональных показателей, а также уменьшение колонизации синегнойной палочки. В связи с отсутствием системного воздействия побочные действия ингаляционной антибактериальной терапии минимальны. Эффективность ингаляционной терапии в большой степени зависит от используемого ингалятора. Сочетание небулайзера и компрессора имеет ряд преимуществ перед ультразвуковым ингалятором. При использовании небулайзера достигается лучшая дисперсия, при которой ингалируемый препарат проникает в нижние дыхательные пути; кроме того, ультразвуковой ингалятор несколько нагревает препарат, что может изменить свойства антибиотика. Ежедневное лечение больного МВ должно выглядеть так: процедуры начинаются с ингаляции бронходилататора, если это показано; затем — ингаляции и/или таблетированный прием муколитика; через 10 — 15 мин — кинезитерапия, откашливание; после паузы — ингаляция антибиотика.
Улучшение нутритивного статуса
очень важно для общего самочувствия пациента и течения инфекционного процесса, развития дыхательной мускулатуры, а в итоге — для прогноза больного МВ [16]. Для его коррекции необходимо:
- выявить экзокринную недостаточность поджелудочной железы;
- проводить постоянную заместительную терапию ферментными препаратами нового поколения. Это — микросферические ферменты с pH-чувствительной оболочкой (креон, панцитрат). Препарат назначается с каждым приемом пищи в дозе до 2000 ед. липазы на 1 кг массы тела больного. Если при подобной дозировке сохраняются симптомы мальабсорбции или есть признаки гиперацидного гастрита, к терапии добавляют блокаторы H2-рецепторов (циметидин, ранитидин) или ингибиторы протонной помпы (омепразол);
- при адекватной заместительной терапии в диете больных МВ не должно быть ограничений. Наоборот, с учетом постоянно текущего инфекционного процесса калораж питания при МВ должен составлять 120 — 150 % от необходимого, 35% из них за счет жиров;
- необходим дополнительный прием витаминов А, Д, Е, К — как правило, назначают двойное количество обычной дневной нормы.
Для предотвращения холестаза рекомендуется постоянный прием урсофалька (уреидодезоксихолиевой кислоты) — гидрофильной желчной кислоты, предотвращающей образование желчных камней;
- при неэффективности перечисленных действий, если у больного значительно уменьшается масса тела, назначают высококалорийные пищевые добавки в форме коктейлей, в дозе, возмещающей 800 ккал/сут для взрослых. При необходимости прибегают к зондовому кормлению в ночное время с использованием пищеводного или желудочного зонда.
Новым направлением в лечении МВ является применение противовоспалительной терапии. Так как бронхиальная обструкция при МВ в большой степени обусловлена гиперактивной воспалительной реакцией, представляется целесообразным применение стероидных и нестероидных противовоспалительных препаратов. В американском исследовании, продолжавшемся 4 года и закончившемся недавно, выявлено значительное улучшение показателей функций внешнего дыхания у пациентов, систематически принимающих ибупрофен, а также уменьшение необходимости антибактериальных препаратов [17]. Кортикостероидные препараты применяются для лечения больных МВ при сопутствующей бронхиальной астме или аллергическом бронхолегочном аспергиллезе. В 4-годичном исследовании по выявлению эффективности системной терапии кортикостероидами в дозе 2 мг/кг через день был получен значительный клинический и функциональный эффект. Однако по отсроченным данным (через 6 лет) были выявлены отставание в росте, остеопороз, катаракта у группы больных, получавших стероиды [18]. Кортикостероидные препараты рекомендуется применять короткими курсами при лечении обострений. В настоящее время исследуется роль ингаляционной стероидной терапии в лечении МВ. Лечение осложнений.
При прогрессировании легочной патологии при МВ развиваются такие осложнения, как гипоксемия, приводящая к легочной гипертензии и развитию легочного сердца. В этом случае проводятся длительная кислородотерапия (в соответствии с показателями газового состава крови), лечение ингибиторами ангиотензинпревращающего фермента (каптоприл, эналаприл), а также традиционное лечение развивающейся недостаточности кровообращения. Выраженное воспаление трахеобронхиального дерева, особенно в зонах бронхоэктазии, часто приводит к легочному кровотечению, которое, однако, редко является непосредственной причиной смерти больного. При неэффективности консервативного лечения рекомендуется проведение ангиографии с эмболизацией бронхиальной артерии или хирургическое вмешательство. Пневмоторакс — это довольно частое осложнение МВ у взрослых, развивающееся из-за разрыва субплевральных булл. После удаления свободного воздуха из плевральной полости при повторных пневмотораксах осуществляется химический или хирургический плевродезис. Сейчас в странах, где проводится трансплантация легких, показания к этой манипуляции сужены.
Трансплантация
является еще одним шансом для больных МВ после того, как ресурсы медикаментозной терапии исчерпаны. Показаниями к трансплантации являются выраженная дыхательная недостаточность с объемом форсированного выдоха в 1 с менее 30%, отсутствие противопоказаний, активное желание больного [19]. При трансплантации производится пересадка обоих легких, возможна также пересадка комплекса легкие — сердце с последующей процедурой «домино», т. е. с пересадкой сердца больного МВ другому реципиенту. В связи с выраженной нехваткой донорских органов иногда проводится пересадка от живых доноров (по одной доле от каждого из родителей), однако эта операция вызывает множество этических возражений и проводится крайне редко [19]. Еще одной надеждой для больных МВ и их врачей является генная терапия [20]. Синтезирован ген белка МВТР, проводятся активные попытки ввести этот ген в эпителиальные клетки бронхов. Доказано, что даже 10% уровень нормального МВТР может обеспечить физиологическую функцию легких. Проведены первые клинические испытания с использованием вектора аденовируса (США, Канада) и липосомами (Англия, Франция). Клинически значимого результата пока не получено [20], однако исследования продолжаются, так как в случае успеха наступит новый этап в лечении МВ — этап этиологического подхода к лечению этого заболевания .
Литература:
1. Andersen DH. Cystic fibrosis of the pancreas and its relation to celiac disease. A clinical and pathologic study. Am J Dis Child 1938;56:344-99. 2. Чучалин А. Г., Самильчук Е. И. Муковисцидоз- — состояние проблемы. Тер. архив — 1993;65;(3):3-8. 3. Hodson ME, Geddes DM (Еds), London: Chapman and Hall, 1995. 4. Потапова О. Ю. Автореферат — Молекулярно-генетический анализ кистозного фиброза в России — С.П. 1994, с. 24. 5. Петрова Н. В., Материалы научно-практической конференции РДКБ — М — 1995, с. 96. 6. Капранов Н. И. Рачинский С. В. Муковисцидоз — М. — 1995. 7. Cystic Fibrosis Foundation. 1995. Patient Registry 1994 Annual Data Report. Bethesda, Maryland. 8. Taussig LM. The reproductive system, in Cystic Fibrosis Brugman, S. M. (Еd. L. M. Taussig), Thieme-Stratton, New York 1984;324-7. 9. Davis PB, et al. Cystic Fibrosis, Am J Respir Crit Care Med 1996;154:1229-56. 10. Warner JO, et al. Cystic fibrosis in children, in Respiratory Medicine (second edition), London 1995:1330-40. 11. van Haren EHJ, et al. Bronchodilator response in adult patients with cystic fibrosis: effects on large and small airways. Eur J Respir Dis 1991;4:301-7. 12. Govan JWR, et al. Evidence of transmission of Pseudomonas cepacia by social contact in cystic fibrosis. Lancet 1993;342:15. 13. Hodson ME. Aerosolized dornase alfa (rhDNase) for therapy of cystic fibrosis. Am J 1995;151:70-4. 14. Pryor JA and Webber BA. Physiotherapy for cystic fibrosis-which technique? Physiotherapy 1992;78:105-8. 15. Webb AK. The treatment of pulmonary infection in cystic fibrosis Scand J Infect Dis Suppl 1995;96:24-7. 16. Cysyic Fibrosis Trust. Management of cystic fibrosis in adults UK 1995. 17. Konstan MW, et al. 1995 Effect of high-dose ibuprofen in patients with cystic fibrosis. 18. Niolaizik WH, MH. Schoni, 1996 Pilot study to assess the effect of inhaled corticosteroids on lung function in patients with cystic fibrosis J Pediatr 128:271-4. 19. Kotloff, Zuckerman. Lung transplantation for cystic fibrosis: special considerations Chest March 1996;109(3):787-98. 20. Southern KW. Gene therapy for cystic fibrosis: current issues. Brit J Hosp Med 1996;55(8):495-9.
Этиология муковисцидоза
Хотя существует немало разновидностей болезни в зависимости от пораженного органа, рассмотри основные. Классификация включает несколько форм.
Поражения поджелудочной железы
Кистозный фиброз поджелудочной железы – муковисцидоз, при котором нарушение выработки секрета происходит в этом важном органе. Вещество, продуцируемое этой железой, содержит комплекс ферментов, участвующих в процессах пищеварения. Когда выработка этого секрета нарушается, выделение из продуктов полезных веществ становится невозможным. В итоге даже самая питательная и полезная пища проходит транзитом и не снабжает организм ценными соединениями.
Когда страдает печень
Один из видов патологии – это, когда поражается печень. Именно в этом органе продуцируется желчь. Повышение ее густоты приводит к застою и тяжелым последствиям. Такие проблемы опасны, но, к счастью, печень при муковисцидозе затрагивается только в 4% случаев.
Поражение дыхательных путей
Стенки бронхов, легких и других частей дыхательных путей покрыты слизистой оболочкой. Выделение секрета происходит постоянно и это необходимо для того, чтобы из организма своевременно выводились инородные частички в виде пыли и патогенных микроорганизмов.
Когда муковисцидоз протекает в легочной форме, вовлекая в процесс дыхательные пути, происходит застой мокроты в бронхах и легких, что приводит к оседанию на стенках органов бактерий, вирусов, пыли. Мельчайшие бронхи подвергаются полной закупорке, что приводит к обструктивным состояниям и нарушает полноценную вентиляцию легких.
Поражение половых органов
Жалобы на работу половых органов при муковисцидозе у женщин не наблюдается. Патология не влияет на работу репродуктивной системы.
У мужчин заболевание поражает яички. В этих органах продуцируется сперма. При нарушении этих процессов мужчины становятся бесплодными. Это происходит в результате закупорки половых протоков.
Изменения в работе потовых желез
При муковисцидозе пот у пациентов становится чрезмерно соленым и липким. Анализ покажет повышенное содержание хлора и натрия.
Поражение желудочно-кишечного тракта
Кишечная форма муковисцидоза встречается часто. Дети с данной патологией страдают от неполноценного расщепления продуктов питания. Слабее всего усваиваются жиры и белки, относительно нормально организм принимает углеводы.
При поражении органов пищеварения внутри тракта начинаются гнилостные процессы. Ненормальный распад продуктов приводит к образованию токсических соединений, которые отравляют организм. Стул становится частым, известны случаи выпадения прямой кишки.
Когда муковисцидоз протекает по кишечному типу, изменяется и состав слюны. Пережевывать сухую пищу становится очень сложно и пациентам приходится все запивать обильным количеством воды. Все эти нарушения постепенно приводят к расстройствам питания, снижению массы тела.
Мекониевая непроходимость
Меконий – это первородный кал. При муковисцидозе иногда проявление болезни начинается с первых дней жизни.
Когда меконий становится слишком вязким, он перекрывает кишечные ходы. Родители могут заметить, что у малыша не отходит кал. Через сутки ребенок становится беспокойным, часто срыгивает, а живот вздувается. Возможна рвота с примесями желчи. На коже живота становится четким сосудистый рисунок, кожа становится сухой и дряблой.
Проводится анализ на иммунореактивный трипсин. Оказывается, что этого фермента нет, поэтому в петлях тонкого кишечника происходит закупорка. Слизь густеет, и появляются все вышеописанные признаки. Устранить данную проблему можно только хирургическим путем.
Особенности смешанного течения
Смешанная форма муковисцидоза сочетает в себе признаки нескольких типов течения. Болезнь начинает проявляться с тяжелых бронхитов и воспалений легких, а затем присоединяется кишечный синдром.
Чем раньше врачу удалось диагностировать муковисцидоз и оказать первую помощь, тем больше шансов на благоприятный исход.
Симптомы муковисцидоза. Диагностика у детей
Большинство случаев муковисцидоза выявляется в первые два года жизни ребенка. Заподозрить заболевание можно по следующим признакам:
- частый, постоянно возобновляющийся кашель, одышка;
- рецидивирующая или хроническая пневмония;
- неоформленный, обильный, маслянистый и зловонный кал;
- хроническая диарея;
- выпадение прямой кишки;
- затяжная неонатальная желтуха;
- отставание в физическом развитии;
- постоянно соленый вкус кожи;
- отеки;
- деформация пальцев по типу «барабанных палочек»;
- увеличенная печень и нарушенная ее функция.
Фото: Jerry Nick / wikimedia.org
Для диагностики муковисцидоза проводят:
- сбор семейного анамнеза и ДНК-пробу (дорогостоящая процедура);
- потовый тест (с помощью специальных анализаторов определяют содержание ионов натрия и хлора в поте);
- анализ крови на уровень иммунореактивного трипсина (при муковисцидозе этот фермент поджелудочной железы выше нормы в 5-10 раз);
- могут назначить обследование, позволяющее обнаружить нарушение функции тех или иных органов из-за муковисцидоза (например, легких, ЖКТ).
Симптоматика муковисцидоза
Так как при муковисцидозе поражаются сразу несколько систем одновременно, симптоматика может быть весьма разнообразной. Первое обострение зачастую происходит именно в первый год жизни, поэтому родители должны чутко следить за самочувствием ребенка и при возникновении отрицательных симптомов сразу же показать малыша специалисту.
Важно! Всего в 10% случаев болезни симптомы проявляются в первые дни жизни, имея при этом самый неблагоприятный прогноз.
Симптомы у новорожденных
Когда муковисцидоз проявляется в грудном возрасте, у малыша появляются симптомы непроходимости кишечника, что связано с застоем мекония:
- отсутствие дефекации;
- надрывный плач;
- вздутие живота.
При пальпации можно нащупать вздутую кишку. Прикосновения причиняют ребенку боль, и плач становится сильнее.
Симптомы у детей до года
В этом возрасте патология диагностируется довольно часто. Основные признаки муковисцидоза в этот период – медленная прибавка в весе и проблемы с дыхательными путями.
Важно! Говорить о наличии этого генетического заболевания можно только в том случае, если нарушения есть одновременно в двух системах, а не только лишь в чем-то одном.
Лечить патологию придется, если есть такой комплекс симптомов:
- нестабильность консистенции кала;
- изменение цвета на желтый;
- обретение жирной консистенции;
- постоянный сухой кашель, усиливающийся во время ночного сна;
- приступы удушья на фоне закупорки мелких бронхов;
- частые респираторные заболевания.
Без оказания помощи периоды обострения будут происходить все чаще.
Симптомы в зависимости от пораженной системы
Раннее обследование ребенка позволяет подобрать лечение, с помощью которого можно контролировать течение заболевания и поддерживать нормальное самочувствие. Признаки болезни могут отличаться в зависимости от того, какая система подверглась патологическому процессу.
При поражении пищеварительной системы могут наблюдаться такие симптомы:
- медленное физическое развитие на фоне неполучения питательных веществ с пищей;
- нарушения стула;
- увеличение селезенки;
- слабость;
- тошнота;
- головная боль;
- отеки разной локализации.
Реже возникает сахарный диабет.
При поражении дыхательной системы интенсивность симптомов нарастает по мере прогрессирования стадии:
- спадание некоторых участков легкого из-за частичной закупорки бронхов;
- сухой кашель;
- кровохарканье;
- одышка;
- бледность кожных покровов;
- выделение скудной густой слизи.
Если присоединяется бактериальная инфекция, слизь может становиться желтой или зеленой.
Большинство симптомов можно купировать, однако когда адекватная терапия отсутствует, в органах начинаются необратимые изменения.
Общее описание
Муковисцидоз (МВ) в качестве данного определения актуальной патологии, используется в Европе (и, собственно, в нашей стране), в то время как в Канаде, Австралии, США и в других странах его определяют как «кистозный фиброз поджелудочной железы», и именно в таком варианте в наибольшей мере раскрываются особенности его морфологических проявлений. Следует заметить, что данное заболевание является достаточно распространенным, о чем свидетельствуют показатели частоты его возникновения. Так, только по новорожденным в масштабах европейских стран определяется соотношение 1:2500, что, в свою очередь, указывает на то, что заболеть муковисцидозом на 10000 новорожденных шансы имеются как минимум у четверых.
Поражение муковисцидозом происходит с одинаковой частотой вне зависимости от половой принадлежности, то есть в одинаковой мере заболеванию подвержены и мальчики, и девочки. Учитывая тот факт, что речь идет о генетическом заболевании, то следует учитывать, что больными уже рождаются, и заразиться муковисцидозом невозможно. Между тем, заболевание это может длительное время протекать без проявления симптоматики, потому целесообразно рассматривать муковисцидоз у взрослых. Симптомы его диагностируются в таком варианте примерно в 4% случаев, хотя в подавляющем большинстве проявляет себя это заболевание в период первых лет жизни. Учитывая тот факт, что дети рождаются уже с ним, нередко его определяют как наследственный муковисцидоз или муковисцидоз врожденный.
Дети заболевают в том случае, когда от каждого родителя ими получено по одному мутантному гену. Если наследуется только один такой ген, то в этом случае рассматривается его носительство («носители МВ»), при котором соответствующих заболеванию патологий не диагностируется. Учитывая то, что гены, имеющиеся у каждого человека, являются парными, каждый из нас, соответственно, является носителем двух копий каждого из генов (опять же, по одному гену от матери, по одному от отца). Определенные гены лишены возможности нормального функционирования при нарушении их структуры. При подобном нарушении в структуре ген является измененным. Потому для того чтобы развился муковисцидоз (как, собственно, и многие другие генетические заболевания), необходимо получить, как отмечено в изначальном примере, два измененных гена. При носительстве родителями МВ любой ребенок пары может с 25%-ной вероятностью получить от каждого из них измененные гены.
Примерно в 70% случаев рассматриваемого заболевания оно проявляет себя до достижения ребенком двухлетнего возраста. За счет относительно недавнего внедрения в медицинской практике неонатального скрининга выявление муковисцидоза в значительной мере сократилось во времени.
Наследование муковисцидоза
Диагностика
Ранняя диагностика поможет взрослым людям заметить у ребенка патологические изменения и оказать своевременную помощь. Это избавит ребенка от применения ненужных препаратов при лечении ложных бронхитов, пневмоний и других заболеваний.
Вначале доктор внимательно выяснит симптомы, которые проявились. Классический анализ крови и мочи не дадут никаких результатов. Для получения достоверных сведений проводятся потовые пробы. При наличии патологии в поте будут содержаться повышенные дозы хлора и натрия. Иногда показатели превышают норму в 3-5 раз.
При наличии сомнений может быть проведена генетическая экспертиза на выявление дефекта гена. После этого для постановки диагноза сомнений нет.
Реже проводятся такие исследования:
- биохимия крови;
- копрограмма;
- анализ мокроты;
- рентген;
- МРТ;
- КТ;
- бронхоскопия.
Какие исследования проводить, решает лечащий врач.
Что это за наследственная болезнь муковисцидоз
Муковисцидозом (МВ) называют мутацию одного гена, передающуюся наследственно и провоцирующую сгущение секрета и закупорку протоков всех жизненно-важных органов. Болезнь была впервые диагностирована американским врачом Дороти Андерсен в 1938 году. А истинная причина заболевания — мутированный ген, определена лишь в 1989 году.
Данный ген (муковисцидозный трансмембранный регулятор) у здорового человека контролирует межклеточную транспортировку таких ионов, как хлор и натрий. У больного человека их регулировка нарушена. Благодаря этому секрет, выделяемый органами, становится гуще и не может выполнять свои функции.
Пробки из секрета, образовавшиеся в протоках являются отличной средой для размножения болезнетворных микроорганизмов. Вследствие чего иммунитет человека сильно снижается, он регулярно и тяжело болеет и без лечения не может вести полноценную жизнь. Также это ведет к формированию полых полостей или содержащих жидкость (то есть кист). Поэтому муковисцидоз нередко называют кистозным фиброзом (Cystic Fibrosis).
Есть у заболевания и еще одно более странное название — болезнь соленого поцелуя, муковисцидоз в 18-19 веках так называют потому, что мать, поцеловав больного ребенка, ощущала на губах привкус соли, а бабки-повитухи таким деткам пророчествовали недолгую жизнь.
Наиболее подвержены заболеванию европейцы, особенно дети и подростки. Согласно статистическим данным около 5% всех больных муковисцидозом — это люди от 40 лет. Заболевание достаточно распространенное. Только в России один из 8000 новорожденных имеет мутировавший ген. В настоящее время патологию можно выявить еще в период внутриутробного развития на неонатальных скринингах. Но чаще муковисцидоз выдает себя в течение первых лет жизни ребенка.
Само заболевание не опасно для окружающих. Если больной принимает соответствующие лекарства, то он может заводить семью и детей, которые при правильном подходе рождаются здоровыми.
Данный ген находится в седьмой паре хромосом. Если мутировала одна хромосома из пары, то человек здоров, но является носителем патологии для своих потомков. Если оба родителя являются больными или носителями, то мутация гена у ребенка неизбежна.
Лечение
Полностью избавиться от муковисцидоза невозможно, так как исправлять нарушенные гены медицина еще не научилась. Лечение заключается в применении средств, оказывающих поддерживающее воздействие на органы и системы. Следовательно, терапия симптоматическая.
Крайне важна диета. При кормлении новорожденных детей лучше отдать предпочтение грудному молоку, так как оно содержит все необходимые вещества и хорошо усваивается организмом. При нарушении выработки ферментов поджелудочной железы, их дают ребенку в виде гранул. Подходят такие препараты, как «Эрмиталь», «Креон» и «Панзинорм».
Важно! Кормить детей с муковисцидозом следует только по требованию: плач, сменяющийся затишьем, а затем снова плач.
В более старшем возрасте важно следить за калорийностью. Рацион должен содержать большее число калорий, так как многое не усваивается организмом больного. Могут быть назначены ферменты и витаминные комплексы.
При поражении дыхательной системы лечение в домашних условиях включает в себя применение таких лекарств:
- «Ацетилцистеин»;
- «Амброксол»;
- «Лазолван»;
- «Карцистеин».
Постоянное применение этих средств позволяет пациентам нормально отхаркивать скопившуюся слизь. Могут потребоваться бронхорасширяющие средства типа:
- «Сальбутамол»;
- «Фенотерол»;
- «Беродуал».
Для выбора препарата лучше проконсультироваться с врачом. Он порекомендует средство, которое будет максимально комфортным в использовании и лучше всего подойдет для конкретной возрастной категории.
Лечение народными средствами также может дать положительный результат. Одна из эффективных методик – кинезитерапия. Другими словами, это «лечение движением». Этот народный способ заключается в выполнении комплекса дыхательных упражнений, позволяющих без медикаментов улучшить состояние больного. Комплекс включает:
- перкуссионный массаж грудной клетки;
- активное глубокое дыхание;
- постуральный дренаж (откашливание в положении, когда голова ниже уровня тела).
Важно строго соблюдать рецепт врача, даже если какие-то рекомендации кажутся малозначительными.
Диагностика заболевания: скрининг новорожденных, генетические исследования
Долгое время единственной возможностью поставить диагноз были потовые пробы. Сегодня все чаще прибегают к генетическим исследованиям. С 2007 года в нашей стране все новорожденные еще в роддоме проходят обязательный неонатальный скрининг на пять наиболее тяжелых наследственных недугов, среди которых и муковисцидоз. Провести исследование можно и во время беременности. Но речь идет лишь о попытке ранней диагностики муковисцидоза, которая, бесспорно, важна, для назначения адекватной терапии, но само заболевание от этого не проходит. Оно наследственное и неизлечимое.
Продолжительность жизни больных муковисцидозом сильно отличается в разных странах. Так, в Америке на сегодняшний день средний показатель – 48 лет. Однако это скорее исключение, чем правило. Этого удалось добиться благодаря титаническим усилиям и слаженной работе врачей, ученых и общественных организацией. С муковисцидозом в России пытаются также активно бороться. Однако этих усилий недостаточно, что подтверждает статистика — в нашей стране больные муковисцидозом живут в среднем на 10-15 лет меньше.
Вот такие памятки можно встретить в американских больницах. В них кратко дана вся важная информация о болезни – симптомы, а также необходимое для больного лечение
ПРОЙТИ ТЕСТ NEXTGEN21
Можно ли предотвратить патологию
Не существует специфической профилактики данного заболевания. Если в семьях мужа и жены были случаи заболевания муковисцидозом, при беременности или еще до ее наступления необходимо обратиться в центры, проводящие генетические обследования и выявить наличие данного гена. Как показано на фото, может быть взята пункция амниотической жидкости, либо же кусочек ткани хориона. Это позволит исследовать ДНК еще не рожденного ребенка.
Грамотные действия врачей и родителей с первых дней жизни позволят обеспечить ребенку нормальную жизнь, насколько это возможно при таком диагнозе.
Смотрите видео:
Диагностика муковисцидоза
Для диагностики муковисцидоза могут понадобиться как лабораторные, так и генетические обследования. Генетические исследования обладают высокой информативностью и позволяют заподозрить развитие болезни почти сразу после рождения. На данный момент обнаружить заболевание можно еще до рождения ребенка при неонатальном скрининге.
Для того, чтобы с уверенностью говорить о наличии у человека муковисцидоза, врач должен диагностировать следующие показатели1,2:
- наличие пороков бронхов или присутствие в бронхах густой и вязкой мокроты;
- положительные результаты потового теста;
- наличие ферментной недостаточности поджелудочной железы;
- случаи муковисцидоза в семье.
Как развивается заболевание
Для нормального функционирования дыхательной и пищеварительной системы органам требуется слизь. Ее роль в работе этих систем огромна: слизь защищает органы и слизистые оболочки от пересыхания, не позволяет размножаться патогенным микроорганизмам, создает комфортную среду для хорошей микрофлоры.
Дефицит влаги в межклеточном пространстве приводит к уменьшению продуцирования слизи.
В норме слизь должна присутствовать в бронхах, покрывая всю внутреннюю поверхность и защищая ее. При попадании с воздухом пыль, грязь, микроорганизмы, чужеродные частицы оседают на слизи, постепенно выводятся из бронхиального дерева с помощью кашля или чиханья.
Если количество вырабатываемой слизи недостаточное, первым делом страдает реснитчатый эпителий. Когда микроорганизмы оседают в бронхах, то начинают использовать реснитчатый эпителий в качестве пищи.
Это приводит к воспалительным заболеваниям, сужению просвета бронхов, спаданию альвеол и как следствие – застою слизи.
Профилактика
Что касается профилактики муковисцидоза, то одним из самых важных мероприятий по предупреждению заболеваемости считается пренатальная диагностика, с помощью которой можно выявить наличие дефекта в седьмом гене еще до наступления родов. Для укрепления иммунитета и улучшения жизненных условий всем больным необходим тщательный уход, полноценное питание, соблюдение личной гиены, умеренная физическая нагрузка и обеспечение максимально комфортных условий для проживания.
Чумаченко Ольга, педиатр
11, всего, сегодня
(153 голос., средний: 4,55 из 5)
Водянка головного мозга у новорожденных – причины развития, симптомы и методы лечения
Гиперактивный ребенок: норма или заболевание?
Похожие записи
Лечения муковисцидоза
Лечения производится с помощью ингаляций и антибиотиков
При диагностировании и начале лечения муковисцидоза на ранней стадии появляется возможность значительно улучшить качество и повысить продолжительность жизни больного. Терапия направлена на применение лечебной диеты, дыхательной гимнастики, прием лекарственных препаратов, выполнение физических упражнений и другие процедуры.
Общего лекарства от муковисцидоза нет. При легочных инфекциях назначаются антибиотики, которые могут быть вводиться внутривенно, путем вдыхания или приниматься перорально. Иногда при лечении муковисцидоза длительно может назначаться антибиотик азитромицин. Полезны и эффективны ингаляции с гипертоническим солевым раствором и сальбутамолом. В тяжелых случаях полной утраты функций легкими вариантом лечения может стать их трансплантация.
В детстве крайне важным является прием препаратов, заменяющих панкреатические ферменты и жирорастворимые витаминные добавки. Лечащим врачом могут быть назначены физиотерапевтические процедуры на грудной клетке.
Прогноз и профилактика
Ранее с проявлениями муковисцидоза сталкивались в основном педиатры, эта болезнь считалась «детской». В настоящее время эта патология нередко встречается и у взрослых, что объясняется возросшими возможностями современной фармакологии. Используемые препараты позволяют частично скомпенсировать нарушенные секреторные функции слизистой оболочки бронхиального дерева и поджелудочной железы. И при адекватно подобранной терапии ребенок с муковисцидозом имеет шанс на взросление.
Важно: перед применением ознакомьтесь с инструкцией или проконсультируйтесь с лечащим врачом.
Как наследуется муковисцидоз
К особенностям наследования муковисцидоза относят:
- Мутация SFTR является рецессивной. Это означает, что у человека с нормальным геном в парной хромосоме не будет никаких симптомов муковисцидоза. Таких людей в популяции достаточно много. Они являются носителями заболевания и могут передавать его патологический ген своим детям.
- Передача гена не связана с полом, так что вероятность появления болезни у мальчиков и девочек одинакова.
- Ребенок будет болен муковисцидозом только в том случае, если он унаследует сразу 2 дефектных гена. Такое возможно, если у обоих родителей имеется хотя бы одна хромосома с мутацией в соответствующей области. Вероятность рождения больного ребенка при этом может быть различной (см. таблицу).
| Мать здорова (обе хромосомы без мутации) | Мать носитель (один ген мутантный, другой нормальный) | Мать больна муковисцидозом (оба гена мутантные) | |
| Отец здоров (обе хромосомы без мутации) | В 100% случаев дети здоровы | Вероятность рождения ребенка-носителя 50%, вероятность рождения носителя 50% | Вероятность рождения больного ребенка 0%, все дети будут носителями |
| Отец носитель (один ген мутантный, другой нормальный) | Вероятность рождения ребенка-носителя 50%, вероятность рождения носителя 50% | 25% вероятность рождения больного ребенка, 25% вероятность рождения здорового, 50% — носителя | Вероятность рождения больного ребенка 50%, вероятность рождения носителя 50% |
| Отец болен муковисцидозом (оба гена мутантные) | Вероятность рождения больного ребенка 0%, все дети будут носителями | Вероятность рождения больного ребенка 50%, вероятность рождения носителя 50% | Все дети будут больны муковисцидозом |
Следует понимать, что на вероятность рождения ребенка с муковисцидозом влияет только факт наличия у родителей аномального гена SFTR. Характер (тип) мутации при этом не имеет значения.
Признаки
Проявления заболевания могут сильно отличаться в зависимости от некоторых факторов:
- начало появления первых симптомов;
- возраст пациента;
- продолжительность течения недуга.
Больные муковисцидозом умственно абсолютно полноценны. Среди них есть одаренные и интеллектуально развитые люди. Специалисты выделяют три основных формы муковисцидоза. Наиболее распространённой считается смешанный тип, при котором в процесс вовлекается респираторный и желудочно-кишечный тракт.
Однако в некоторых случаях легочная и кишечная формы могут протекать изолированно. Заболевание редко дебютирует после совершеннолетия. Обычно наблюдается переход патологии из детской формы во взрослую. Симптомы у детей и взрослых схожи. У мужчин и женщин диагностируется бесплодие.
Легочная форма
Для нее характерно постепенное нарастание симптомов. В итоге заболевание приобретает хроническую затяжную форму. У новорожденных рефлексы чихания и кашля еще в полной мере не развиты, поэтому вязкий секрет начинает активно скапливаться в респираторном отделе.
К первым симптомам поражения бронхов относятся кашель с небольшим выделением тягучей слизи, одышка, синюшность кожи, нарушение сна и общего состояния. Симптомы интоксикации отсутствуют. Гипоксия (недостаток кислорода) вызывает задержку в физическом развитии. Дети плохо набирают в весе, они становятся вялыми, апатичными.
О присоединении инфекции говорят следующие симптомы муковисцидоза:
К какому врачу обратиться с кишечником?
- высокая температура;
- кашель с густой гнойной мокротой;
- одышка;
- головная боль;
- тошнота и рвота;
- головокружение;
- нарушение сознания.
Грудная клетка больного приобретает бочкообразную форму. Кожа теряет свою эластичность и упругость, становится сухой. Наблюдается выпадение волос. Они теряют свой блеск и становятся ломкими. При длительном течении поражается и носоглотка. К вышеупомянутым симптомам добавляются синуситы. Полипы, аденоиды, хронические тонзиллиты.
Со временем развивается симптом «барабанных палочек» и «часовых стекол». Из-за легочной недостаточности деформируются фаланги пальцев и ногтевые пластины. Выделяют четыре основных стадии развития бронхолегочного муковисцидоза:
- Присутствует упорный сухой кашель. Одышка появляется исключительно при физической нагрузке. Первая стадия может длиться до десяти лет.
- Сухой кашель переходит во влажный. Присутствует хронический обструктивный бронхит. Одышка появляется даже при умеренной физической нагрузке.
- Формируются осложнения муковисцидоза. Развивается легочно-сердечная недостаточность.
- Длится всего несколько месяцев и заканчивается летальным исходом.
На фото отчетливо видно, как выглядят легкие при муковисцидозе
Микразим при муковисцидозе
Применение ферментных препаратов при муковисцизоде позволяет частично скомпенсировать недостаточный уровень собственных пищеварительных ферментов. А такие нарушения отмечаются практически у всех людей с этим заболеванием, ведь поражение поджелудочной железы является его типичным проявлением. Особого внимании при этом требует коррекция уровня липазы – фермента, обеспечивающего адекватного переваривание жиров в тонком кишечнике. С этой целью при муковисцидозе назначается Микразим.
К ожидаемым клиническим эффектам такой терапии относят:
- Улучшение усвоения базовых нутриентов, снижение вероятности алиментарной гипотрофии.
- Уменьшение риска развития диареи, связанной с недостаточным перевариванием жиров.
- Снижение выраженности кишечного дискомфорта, обусловленного повышенным газообразованием и усиленной перистальтикой на фоне ферментной недостаточности.
Микразим при муковисцидозе может быть использован и для лечения детей первых лет жизни, в этом случае препарат назначается в виде капсул. Дозировка подбирается врачом с учетом выраженности стеатореи и возраста ребенка.
Симптомы
Муковисцидоз в большинстве случаев проявляется до годовалого возраста.
В 10% случаев симптомы заболевания (мекониевая непроходимость кишечника или мекониальный илеус) обнаруживаются при ультразвуковом исследовании еще в период внутриутробного развития во 2-3 триместре.
У части детей кишечная непроходимость обнаруживается в первые дни жизни. Признаками мекониального илеуса являются:
- отсутствие физиологического выделения мекония;
- вздутие живота;
- беспокойство;
- срыгивания;
- рвота, при которой в рвотных массах обнаруживается присутствие желчи.
На протяжении двух дней состояние ребенка ухудшается — появляется бледность и сухость кожных покровов, снижается тургор тканей, появляется вялость и адинамия. Развивается обезвоживание и нарастает интоксикация. В некоторых случаях возможно развитие осложнения (перфорация кишечника и перитонит).
Кишечный муковисцидоз проявляется в большинстве случаев после введения прикорма или искусственного вскармливания благодаря недостаточности панкреатических ферментов. Симптомами данной формы заболевания являются:
- вздутие живота;
- частые дефекации
- значительно увеличенное выделение кала;
- зловонность и светлый цвет кала, присутствие в нем значительного количества жира.
Возможно выпадение прямой кишки при высаживании на горшок (наблюдается у 10-20% больных).
Часто присутствует ощущение сухости во рту, возникающее из-за вязкости слюны, поэтому прием сухой пищи затруднен, и в процессе еды больные вынуждены в большом количестве употреблять жидкость.
Аппетит на начальных этапах может быть повышен или соответствовать норме, но благодаря нарушениям пищеварения впоследствии развивается гиповитаминоз и гипотрофия. В процессе развития заболевания присоединяются признаки цирроза и холестатического гепатита (повышенная утомляемость, похудание, желтуха, потемнение мочи, нарушения поведения и сознания, боли в животе и др.).
Муковисцидоз легких благодаря гиперпродукции в бронхолегочной системе вязкого секрета вызывает обструктивный синдром, который проявляется:
- удлинением выдоха;
- появлением свистящего шумного дыхания;
- приступами удушья;
- участием в дыхательном акте вспомогательной мускулатуры.
Возможен малопродуктивный кашель.
Инфекционно-воспалительный процесс носит хронический рецидивирующий характер. Наблюдаются осложнения в виде гнойно-обструктивного бронхита и тяжелых пневмоний со склонностью к абсцедированию.
Симптомами легочной формы заболевания являются:
- бледно-землистый оттенок кожи;
- вызванная недостаточным кровоснабжением синюшная окраска кожи;
- наличие одышки в состоянии покоя;
- бочкообразная деформация грудной клетки;
- деформация пальцев рук (концевые фаланги напоминают барабанные палочки) и ногтей (напоминают часовые стекла);
- пониженная двигательная активность;
- снижение аппетита;
- низкая масса тела.
Симптом барабанных палочек и часовых стекол при муковисцидозе.
Бронхиальное содержимое обычно включает синегнойную палочку, золотистый стафилококк и гемофильную палочку. Флора может проявлять устойчивость к антибиотикам.
Легочная форма оканчивается летальным исходом в связи с тяжелой дыхательной и сердечной недостаточностью.
Признаки муковисцидоза при смешанной форме включают симптомы кишечной и легочной форм. Стертые формы заболевания диагностируются обычно в зрелом возрасте, поскольку особые разновидности мутаций в гене CFTR вызывают более легкое течение болезни, а ее симптомы совпадают с симптомами синусита, рецидивирующего бронхита, хронических обструктивных болезней легких, цирроза печени или мужского бесплодия.
Муковисцидоз у взрослых часто вызывает бесплодие. У 97 % мужчин, больных муковисцидозом, выявляется врожденное отсутствие, атрофия или обструкция семенного канатика, а у большинства страдающих муковисцидозом женщин наблюдается снижение фертильности из-за повышенной вязкости слизи цервикального канала. При этом у части женщин детородная функция сохраняется. Также иногда встречаются мутации гена CFTR у мужчин, не имеющих признаков муковисцидоза (следствием мутации в 80% таких случаев является аплазия семявыносящего протока).
На умственном развитии муковисцидоз не сказывается. Тяжесть течения заболевания и его прогноз зависят от сроков манифестации болезни – чем позже проявились первые симптомы, тем легче протекает заболевание и тем благоприятнее прогноз.
Поскольку муковисцидоз благодаря большому количеству вариантов мутаций отличается полиморфизмом клинических проявлений, тяжесть заболевания оценивают по состоянию бронхолегочной системы. Выделяются 4 стадии:
- 1-я, для которой характерны непостоянные функциональные изменения, сухой кашель без отделения мокроты, незначительная или умеренная одышка при физических нагрузках. Длительность первой стадии может достигать 10 лет.
- 2-я стадия, для которой свойственно развитие хронического бронхита, наличие кашля, сопровождающегося отделением мокроты, умеренная в покое и усиливающаяся при напряжении одышка, деформация концевых фаланг пальцев. При выслушивании выявляется наличие жесткого дыхания с влажными, «трескучими» хрипами. Данная стадия длится от 2 до 15 лет.
- 3-я стадия, на которой возникают осложнения и прогрессирует патологический процесс в бронхолегочной системе. Происходит формирование бронхоэктазов, зон диффузного пневмофиброза и ограниченного пневмосклероза, кист. Наблюдается сердечная недостаточность (правожелудочковый тип) и выраженная дыхательная недостаточность. Продолжительность стадии составляет от 3 до 5 лет.
- 4-я стадия, для которой характерна тяжелая кардио-респираторная недостаточность, оканчивающаяся летальным исходом в течение нескольких месяцев.